Mitos frecuentes: Limpieza desinfectante en ambientes controlados
Puntos clave:
- Los datos de monitoreo ambiental (EM) no siempre predicen confiablemente el riesgo de contaminación, ya que corresponden a un punto temporal, y es posible que no se correlacionen con la exposición real del producto o el estado del proceso aséptico.
- Los residuos de desinfectantes no son intrínsecamente peligrosos para la calidad del producto, y la creencia de que los residuos albergan microorganismos viables carece de bases científicas; un enfoque basado en riesgos debe guiar el manejo de los residuos.
- La pulverización de desinfectantes no es automáticamente mejor que limpiar con un trapo/toallita o trapear, ya que la eficacia depende de lograr la cobertura total de la superficie, y la acción mecánica de la limpieza con trapo/toallitas puede mejorar la eliminación de microbios.
- Aunque el uso rutinario de desinfectantes y esporicidas es esencial para mantener el control en salas blancas, se deben evaluar de forma crítica las premisas sobre sus limitaciones, como la aparición de resistencia o la interferencia de residuos.
- Las estrategias de aplicación de desinfectantes se deben adaptar a factores específicos de la instalación, incluidos los tipos de superficie, accesibilidad del área y tendencias históricas del EM, en lugar de depender de prácticas generalizadas u obsoletas.
Los mitos y malentendidos abundan cuando se trata de microbiología, desde la “regla de los 5 segundos” para comer alimentos que se han caído al piso hasta la tradición popular sobre matar de hambre un resfriado y alimentar una fiebre. Cuando se trata de salas blancas y microbiología farmacéutica, algunos “mitos” están arraigados e incluso los han avalado organismos normativos. Por ejemplo, todavía hay autoridades que insisten en la rotación de desinfectantes para evitar el surgimiento de cepas bacterianas resistentes. El objetivo de los autores de este documento es usar la lógica y ciencia para disipar algunos mitos microbiológicos relacionados con la limpieza desinfectante de ambientes controlados.
Abajo se enumeran algunas creencias, prácticas y políticas cuestionables que encontramos:
MITO: Los datos de monitoreo ambiental (EM) son predictores confiables de riesgos para la calidad de los productos.
HECHO: Los datos de EM de microbios viables generalmente reflejan un momento dado, lo que es una condición transitoria que podría persistir o no persistir. Un solo punto de datos (es decir, una muestra de superficie) no se puede extrapolar necesariamente como relevante más allá de sus parámetros de muestra inmediatos. Los autores han sido testigos de simulaciones de procesos asépticos contaminados (llenado de medios) en los que el EM correspondiente resultó totalmente limpio (0 unidades formadoras de colonias [UFC]). A la inversa, hemos visto resultados de aprobación de un llenado de medios en el que los datos de EM mostraron contaminación aberrantemente alta, con múltiples desviaciones de niveles de alerta y acción. La interpretación de datos de EM de salas blancas es una práctica con muchos matices y lo óptimo es que la realice personal con capacitación, estudios y experiencia adecuados.
MITO: Los residuos secos de desinfectantes en las superficies son intrínsecamente riesgosos para la calidad de los productos farmacéuticos.
HECHO: Cualquier residuo superficial, en las condiciones adecuadas, puede suponer un riesgo para la calidad. La teoría de que los residuos desinfectantes pueden albergar microorganismos viables es una idea no comprobada y más bien contraria a la lógica cuando se consideran las necesidades metabólicas de microorganismos viables. La única forma de proceder aconsejable es una estrategia basada en los riesgos y la ciencia para abordar los residuos desinfectantes o cualquier otro residuo de salas blancas.
MITO: Con la pulverización de desinfectantes sobre superficies se logra cobertura superior y, de tal suerte, mayor eficacia que al trapear o pasar un trapo o toallita. HECHO: ¡La técnica es importante! Los desinfectantes químicos líquidos funcionan gracias al contacto directo con las membranas celulares. La pulverización puede ser efectiva si se logra cobertura contigua. La acción mecánica de limpiar y trapear también tiene ventajas adicionales. Comparar los dos métodos no es un ejercicio sencillo o directo. Las compañías deben considerar muchos factores al determinar el modo óptimo de aplicación en sus procesos e instalaciones, entre ellos los materiales superficiales y la complejidad, tamaño y accesibilidad de las áreas, así como los resultados históricos del EM. Una evaluación de riesgos formal ayuda a determinar la mejor estrategia.
MITO: El material recuperado de mohos de una superficie con le EM requiere una acción correctiva con uso un agente esporicida sobre dicha superficie.
HECHO: Como se menciona arriba, los resultados del EM corresponden a un momento y en general reflejan condiciones transitorias. Dada la separación temporal entre la recolección de la muestra y la recepción de los resultados (lo usual es 3-5 días), es probable que hayan ocurrido muchas actividades en el área, que vuelven ilógico reaccionar como si las condiciones siguieran siendo las mismas. Es frecuente que la superficie en cuestión ya se haya tratado con un detergente germicida que tiene eficacia fungicida. La prevención es mejor que la reacción; la investigación exhaustiva del origen del moho y prevenir su recurrencia es una mejor estrategia y es científicamente más sólida.
Mito: Más es mejor
En numerosas visitas a instalaciones biofarmacéuticas y de dispositivos médicos, los autores han observado el uso de complejos regímenes de desinfección de superficies en salas blancas, con uso de 3 o más variedades de desinfectantes y múltiples tipos de agentes esporicidas. A manera de ejemplo, en varias compañías que visitamos recientemente en Sudamérica se implementan dichos regímenes complejos. Estas estrategias complejas de desinfección de salas blancas pueden ser abrumadoras para los empleados que las implementan, sin beneficios en cuanto al control de la carga biológica. El hecho es que el uso rutinario de un solo detergente germicida de amplio espectro, aunado al uso periódico y dirigido de un agente esporicida, es un programa efectivo de control suficiente de la carga biológica en la gran mayoría de los entornos de salas blancas.1
P: Si los esporicidas matan todo, ¿no deberíamos usarlos todo el tiempo?
R: La inactivación química de las endosporas bacterianas requiere formulaciones muy agresivas, como mezclas de hipoclorito de sodio o peróxido de hidrógeno y ácido peracético/acético (APA). El uso de un esporicida a base de oxidante con frecuencia excesiva puede causar problemas de corrosión en las salas blancas, además de problemas de exposición ambiental, salud y seguridad (EH&S). Por lo tanto, se deben usar con mesura los esporicidas y su frecuencia de uso se debe basar en el riesgo y el material recuperado históricamente de bacterias formadoras de endosporas con el EM.
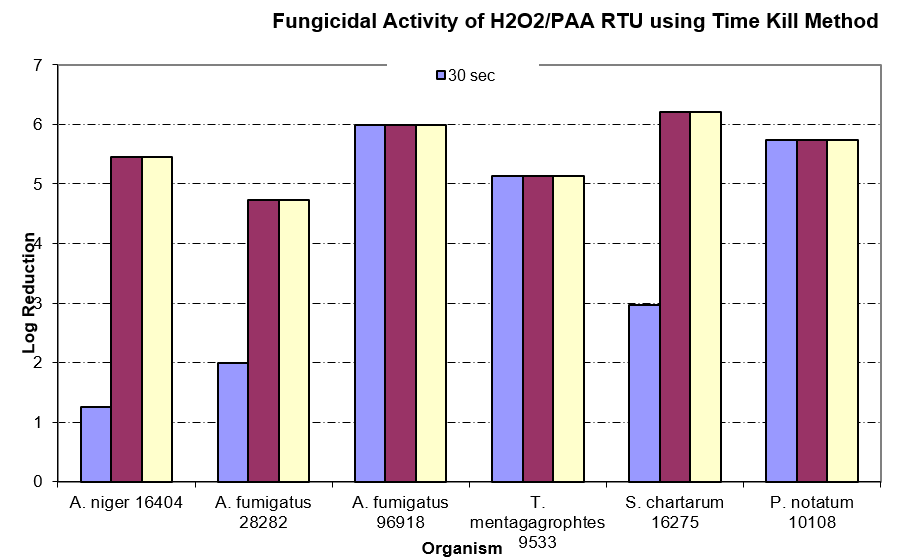
El alcohol es otro agente de salas blancas que no siempre se usa correctamente. En muchas instalaciones solo se alcohol isopropílico (IPA) al 70% en artículos que se transfieren al entorno de sala blanco, con la premisa de que es efectivo contra esporas de hongos y bacterias. Aunque podría tener algo de efecto contra las esporas de hongos, como se muestra en la tabla siguiente (estudio Time-Kill2), se requiere un agente esporicida verdadero para evitar el ingreso de microbios formadores de esporas en las salas blancas
Eficacia del H2O2/PAA listos para usarse (RTU) contra los mohos
Aunque es frecuente que se capacite con los SOP a los usuarios para que usen movimientos superpuestos unidireccionales con trapeadores de cabeza plana en paredes y suelos, esta técnica puede ser contraproducente si la capacitación fue insuficiente y las prácticas no se aplican. Usar las diluciones de uso correctas es otro elemento clave de la desinfección efectiva.3 Los cilindros graduados y los paquetes de dosis unitaria son la forma más exacta. Nunca es aconsejable verter desinfectante concentrado en una cubeta “al tanteo”.
Un programa eficaz de limpieza y desinfección siempre debe contar con un desinfectante de eficacia de amplio espectro y un esporicida para abordar las endosporas bacterianas en las operaciones de sala blanca.

(Image Credit: http://www.pppmag.com/article/714/June_2010/Cleaning_Practices_for_Cleanroom_Contamination_Control/)
Mito: Los residuos de desinfectantes albergarán una carga biológica e interferirán en la eficacia de esporicidas
Se requiere la aplicación rutinaria de agentes desinfectantes y esporicidas para mantener el control ambiental de las salas blancas. El uso rutinario de estos productos puede dejar residuos superficiales. Aunque es posible que surjan problemas debido al uso de productos químicos incompatibles en la rotación, ¿promueven los residuos de desinfectante por sí solos la contaminación microbiana? ¿Interfieren los residuos de desinfectantes en la eficacia esporicida?
Los desinfectantes fenólicos de última generación de STERIS se evaluaron como residuos en un estudio de eliminación temporal para evaluar el impacto en la eficacia de un agente esporicida listo para usarse (RTU) (SporKlenz® RTU) contra Bacillus subtilis, ATCC #19659. Los sólidos (µg/cm2) del desinfectante seco se determinaron en un estudio separado, en el que se calculó la cantidad de residuos después de varias aplicaciones en una probeta de prueba de acero inoxidable de 116 cm2 para imitar el uso típico en salas blancas, así como la cantidad de SporKlenz RTU para cubrir una superficie en aplicaciones típicas de su uso como diluyente. En este último caso, se determinó que 120 mg de esterilizante SporKlenz RTU cubren una probeta de 116 cm2. La proporción determinada en este experimento se extrapoló para determinar la dilución de los residuos de desinfectante en una solución de agente esporicida.
Se añadió un volumen de 0.1 ml de la suspensión de microorganismos a 9.9 ml de la solución de prueba (es decir, el esterilizante Spor-Klenz RTU con un desinfectante fenólico de pH bajo o alto). Se añadió un control de amortiguador usando la misma cantidad. Tras la inoculación, se extrajo una muestra de 0.1 ml luego de 2.5, 5, 7.5, 10 y 20 minutos. Las muestras se neutralizaron, sembraron e incubaron durante 48-49 horas a 37 ± 2 °C. Los organismos viables por mililitro de muestra se determinaron con un recuento de placas aeróbicas estándar.
Reducción logarítmica media de B. subtilis usando residuos fenólicos y solución de agente esporicida
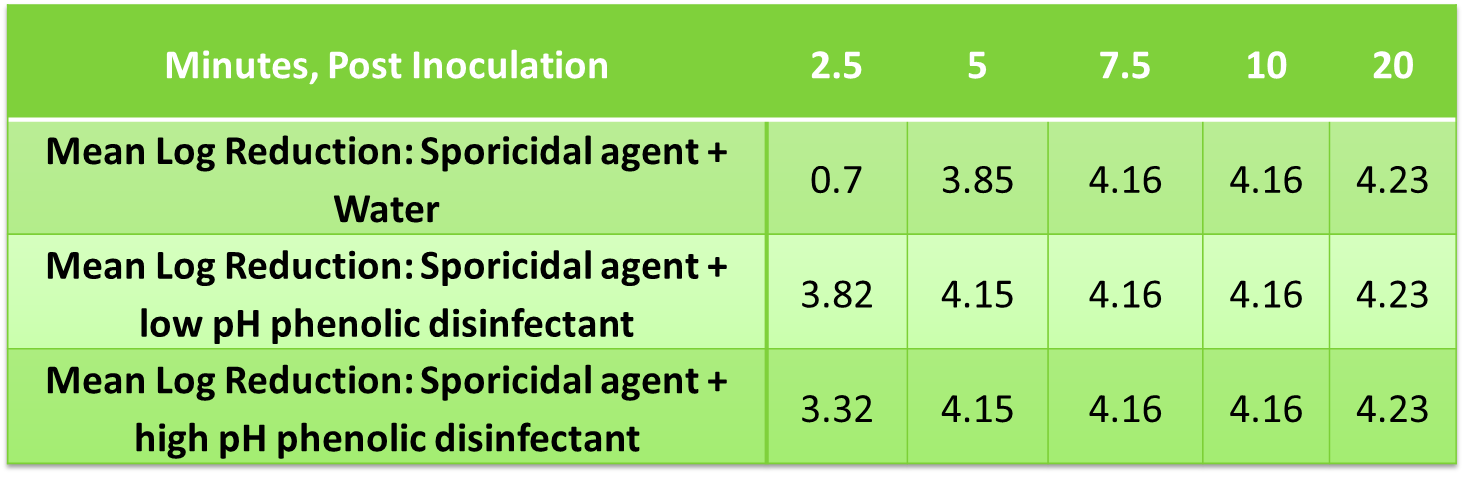
De manera similar, se evaluaron los residuos desinfectantes secos para determinar el efecto sobre la eficacia esporicida, ya que esto refleja prácticas típicas de las salas blancas. Las muestras se prepararon para que correspondieran a 20 días de aplicación de desinfectante a un área conocida, se dejaron secar y luego se trataron con un volumen de agente esporicida suficiente para cubrir el área conocida, u 8.6 µl/cm2. El inóculo se preparó a partir de una suspensión de esporas de Bacillus subtilis, ATCC #19659. La suspensión de esporas de prueba se diluyó con agua desionizada (DI) a aproximadamente 3.0 × 108 UFC/ml. La suspensión se añadió a tubos que contenían muestras de prueba o amortiguador Butterfields para obtener una mezcla al 1 % v/v de microorganismo en producto de prueba o amortiguador. En diversos puntos temporales, las muestras se neutralizaron, sembraron e incubaron por 48-50 h a 37 ± 2 °C después de la inoculación. Los organismos viables por mililitro de muestra se determinaron con el recuento de placas aeróbicas estándar y se transformaron a valores logarítmicos 10 para su análisis.
Reducción logarítmica media de B. subtilis usando residuos fenólicos secos y solución de agente esporicida
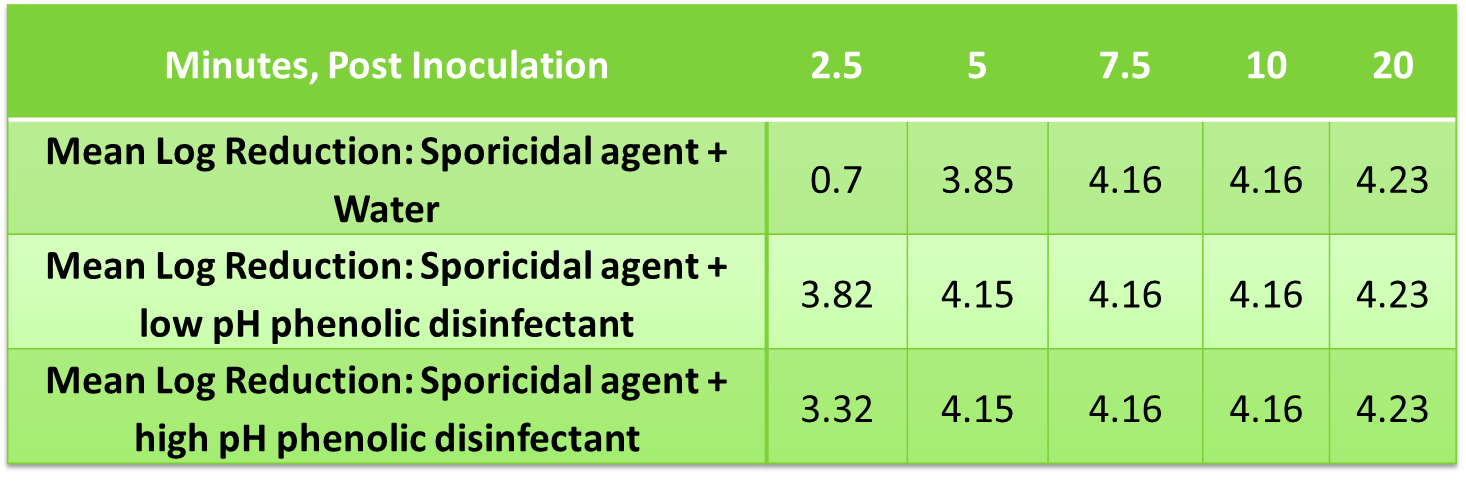
Los datos no muestran efectos inhibidores/antagonistas de los residuos secos con efectividad esporicida.
Capacitación básica
Es lamentable, en las industrias biofarmacéutica, de productos de dosis orales sólidas (OSD) y de dispositivos médicos que el “personal de limpieza”, responsable de la limpieza desinfectante de las áreas de producción de salas blancas reguladas, suele recibir capacitación, guía y supervisión mínimas en comparación con otros departamentos (por ejemplo, control de calidad y fabricación). Muchas veces, en aras del ahorro de costos, la función de limpieza desinfectante se delega en una compañía de limpieza contratada, lo que complica adicionalmente las cuestiones de capacitación y aleja al personal de limpieza de la supervisión del control de calidad (CC) y el aseguramiento de la calidad (AC). Su ejecución fuera de los turnos de producción oscurecen todavía más lo que ocurre en el área de producción. En el mercado global actual, también podría haber barreras lingüísticas que con las que se debe lidiar. Para complicar aún más las cosas, el éxito de la desinfección de superficies y entornos de salas blancas depende enteramente de las habilidades y técnica del usuario. A diferencia de la limpieza física de la residuos visibles, las superficies de las salas blancas normalmente ya parecen estar limpias. Así pues, se pide a los empleados que eliminen materia invisible, trátese de una carga biológica viable o de contaminación por partículas subvisibles. Hay pocas señales visuales, si acaso, que indiquen cuándo una superficie fue descontaminada eficazmente. Es por estas razones que los usuarios a cargo de la limpieza desinfectante deben estar excepcionalmente bien capacitados y conocer los principios de microbiología, control de la contaminación y prácticas asépticas.
Referencias:
- PDA Technical Report No. 70 (2015). Fundamentals of Cleaning and Disinfection Programs for Aseptic Manufacturing Facilities. Available from Parenteral Drug Association, Inc.
- Polarine, J., Macauley, J., Karanja, P., Klein, D., Martin, A. (2009) Evaluating the Activity of Disinfectants Against Fungi. Cleanrooms: The Magazine of Contamination Control Technology 23(2).
- http://www.pppmag.com/article/714/June_2010/Cleaning_Practices_for_Cleanroom_Contamination_Control/
Contenido sugerido
Un proceso justificado para la limpieza y desinfección
Mejores prácticas de validación de desinfectantes en salas blancas
Eliminación de residuos en salas limpias: Una descripción general de la normativa
Únase a nuestra lista de correo electrónico para recibir las últimas novedades del sector y actualizaciones de productos.
Al hacer clic en Suscribirse, confirma que acepta nuestros Términos y condiciones.



